Природные антибактериальные системы молока (часть 4)
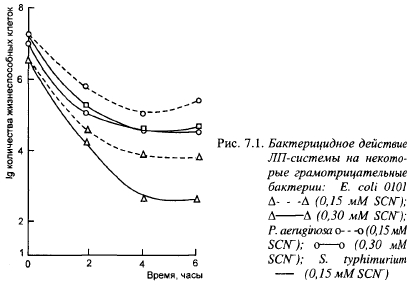
На рис. 7.1 показано бактерицидное действие ЛП-системы на грамотрицательные бактерии в среде, содержащей 1,5 мкг/мл ЛП, 0,15-0,30 мкг/мл SCN и 0,10 мкг/мл глюкозооксидазы (для образования Н2О2).
Египетские ученые использовали лактопероксидазную систему для обработки молока в производстве рассольного сыра Домиати. Они вносили в молоко Н2O2 в количестве 200-250 мг/кг или смесь SCN (14 мг/кг) и Н2O2 (30 мг/кг) с повторным внесением через 4 ч еще 30 мг/кг Н2O2, после чего вырабатывали сыр по обычной технологии. Подобная обработка увеличивала время свертывания и несколько снижала выход сыра. Качество сыров, вырабатываемых из такого молока, было не очень высокого, но приемлемого уровня.
Около 55% активности лактопероксидазы сохраняется в молоке после пастеризации при 72° С в течение 15 с. Следовательно, ЛП-система должна действовать и в пастеризованном молоке.
Stadhouders установил, что скорость кислотообразования 10 мезофильных заквасок в течение 6 ч при 30° С в пастеризованном молоке при 72° С, 15 с была на 14-90% ниже, чем в молоке, пастеризованном при 95° С в течение 30 с (при этом режиме пастеризации ЛП полностью дезактивируется и ЛП-система перестает функционировать). Добавление ЛП к молоку, пастеризованному при 95° С, снижало кислотообразующую активность заквасок до уровня, характерного для молока, пастеризованного при 72° С в течение 15 с. Этот опыт говорит о сохранении активности ЛП-системы в молоке, пастеризованном при установленном в сыроделии режиме. В результате этого опыта была также установлена разная чувствительность заквасок к действию этой системы, что может быть обусловлено неодинаковой активностью NADH Н2О2 оксидазы у штаммов лактококков, входящих в закваски, а от ее активности зависит количество образуемой микроорганизмами Н2О2. Одна из испытанных заквасок в присутствии ЛП не снизила, а повысила скорость кислотообразования. Возможно, микрофлора этой закваски вообще не образовывала свободной Н2O2, а ЛП дезактивирует какие-то перекисные продукты, имеющиеся в молоке, и тем самым стимулирует рост и кислотообразующую активность этой закваски.
- Природные антибактериальные системы молока (часть 3)
- Природные антибактериальные системы молока (часть 2)
- Природные антибактериальные системы молока (часть 1)
- Нитраты
- Пестициды (часть 3)
- Пестициды (часть 2)
- Пестициды (часть 1)
- Микотоксины
- Минеральные компоненты (часть 5)
- Минеральные компоненты (часть 4)
- Минеральные компоненты (часть 3)
- Минеральные компоненты (часть 2)
- Минеральные компоненты (часть 1)
- Лактоза и цитраты
- Молочный жир
- Белки (часть 4)
- Белки (часть 3)
- Белки (часть 2)
- Белки (часть 1)
- Химический состав и основные свойства молока
- Основные понятия молока (часть 2)
- Основные понятия молока (часть 1)
- Психротрофные микроорганизмы (часть 12)
- Психротрофные микроорганизмы (часть 11)
- Психротрофные микроорганизмы (часть 10)
- Психротрофные микроорганизмы (часть 9)
- Психротрофные микроорганизмы (часть 8)
- Психротрофные микроорганизмы (часть 7)
- Психротрофные микроорганизмы (часть 6)
- Психротрофные микроорганизмы (часть 5)
