Свойства молокосвертывающих энзимов (часть 2)
Способность быстро гидролизовать æ-казеин - общее свойство молокосвертывающих энзимов, применяемых в сыроделии, - называют молокосвертывающей активностью, в отличие от способности расщеплять другие связи в белках, получившей название общей протеолитической активности. Общая протеолитическая активность молокосвертывающих энзимов по отношению к молокосвертывающей должна быть как можно более низкой.
Одна часть кристаллического химозина может свернуть 72 млн. частей молока при 35° С. Химозин гидролизует в æ-казеине связь Фен105-МеТ106 в 200 раз быстрее, чем другие связи. Это обусловлено составом и последовательностью расположенных радом с ней аминокислот. æ-Казеины женского и свиного молока вообще не содержат этой связи, но оба гидролизуются говяжьим химозином, хотя и медленнее, чем æ-казеин коровьего молока. По данным Foltman с соавт., говяжий химозин свертывает коровье молоко в два раза быстрее, чем свиное, а свиной химозин свертывает свиное молоко в шесть раз быстрее, чем коровье.
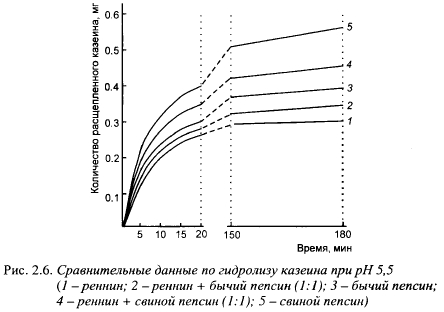
Молокосвертывающие энзимы существенно различаются по отношению общей протеолитической активности к молокосвертывающей. При оптимальном для каждого фермента pH и равной молокосвертывающей активности соотношение общей протеолитической активности (по гемоглобину) говяжьего химозина, говяжьего и свиного пепсина составило 1:3:6. На рис. 2.6 показан гидролиз казеина некоторыми молокосвертывающими препаратами при pH 5,5, близком к pH созревающих сыров и содержимому желудка телят в молочный период. Неспецифический протеолиз (избыточный по отношению к химозину) после 3-часовой инкубации составил для свиного пепсина 0,275 мг, для говяжьего - 0,10 мг, для смеси химозин + говяжий пепсин - 0,05 мг, что соответствовало 87,9; 30 и 12% к протеолизу под действием химозина. Химозин обладает самой низкой общей протеолитической активностью по отношению к молокосвертывающей активности.
- Свойства молокосвертывающих энзимов (часть 1)
- Основные понятия молокосвертывающих энзимов (часть 2)
- Основные понятия молокосвертывающих энзимов (часть 1)
- Мицеллы казеина (часть 7)
- Мицеллы казеина (часть 6)
- Мицеллы казеина (часть 5)
- Мицеллы казеина (часть 4)
- Мицеллы казеина (часть 3)
- Мицеллы казеина (часть 2)
- Мицеллы казеина (часть 1)
- Белки молока (часть 2)
- Белки молока (часть 1)
- Общие понятия коагуляции молока (часть 2)
- Общие понятия коагуляции молока (часть 1)
- Классификация сыров (часть 7)
- Классификация сыров (часть 6)
- Классификация сыров (часть 5)
- Классификация сыров (часть 4)
- Классификация сыров (часть 3)
- Классификация сыров (часть 2)
- Классификация сыров (часть 1)
- Развитие сыроделия в России (часть 8)
- Развитие сыроделия в России (часть 7)
- Развитие сыроделия в России (часть 6)
- Развитие сыроделия в России (часть 5)
- Развитие сыроделия в России (часть 4)
- Развитие сыроделия в России (часть 3)
- Развитие сыроделия в России (часть 2)
- Развитие сыроделия в России (часть 1)
- Возникновение и развитие сыроделия (часть 7)
